Um die Sicherheit und Wirksamkeit von additiv gefertigten Medizinprodukten zu gewährleisten, hat die US-Arzneimittelbehörde FDA ein eigenes Additive Manufacturing Lab eingerichtet. Das Labor ist Teil des Office of Science and Engineering Laboratories (OSEL) innerhalb der FDA.
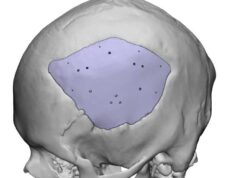
In den letzten zehn Jahren hat sich die additive Fertigung von einer Nischentechnologie zu der bevorzugten Produktionsmethode für Hörgeräte und Metall-Wirbelsäulenimplantate entwickelt. Bislang hat die FDA über 100 Zulassungen für additiv gefertigte Medizinprodukte erteilt. Weitere orthopädische, zahnmedizinische und diagnostische Anwendungen nutzen bereits die Technologie. Laut FDA wurde das volle Potenzial der additiven Fertigung aber noch nicht ausgeschöpft.
Mit dem neuen Labor will die Behörde regulatorische Fragen klären, um so Innovationen in Medizinprodukten hinsichtlich Design, Materialien und Fertigung anzukurbeln.
Zu den Kernherausforderungen zählt die FDA beispielsweise die unzureichende Validierung und das Monitoring von additiven Fertigungsprozessen sowie damit verbundene Unsicherheiten bei der Leistungsvorhersage von Medizinprodukten. Eine konstante Weiterentwicklung von Hard- und Software erschwert dabei angemessene Anpassungen bei Zulassungsprüfungen.
Das übergeordnete Ziel des Additive Manufacturing Program ist es, Wissenslücken bezüglich der Technologie zu schließen und so die Bewertung des Nutzen-Risiko-Verhältnisses zu verbessern. Zudem geht es um eine bessere FDA-Vorbereitung auf Fragestellungen rund um additive Fertigung – und zwar sowohl vor als auch nach der Markteinführung.